2025-04-03 10:54:17
- HLA/MHC(Human)——人的MHC即称HLA
HLA(human leucocyte antigen,人类白细胞抗原)是一组呈高度多态性的基因群。人类的HLA基因编码的产物称为MHC(major histocompatibility complex,主要组织相容性复合体),分布于不同类型的细胞表面,不但决定着宿主的组织相容性,而且决定了个体对不同抗原产生免疫应答的能力。HLA是位于人6号染色体短臂上的一段约3.6M的参与免疫反应的多态性区域。HLA的功能有两方面:一个就是组织特异性抗原;另外一个是抗原呈递。
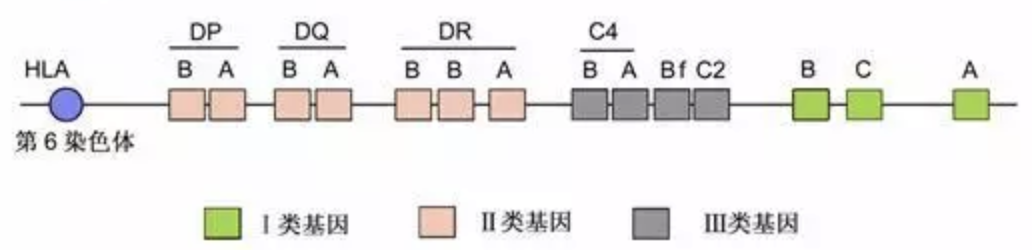
图:HLA结构
HLA复合物是由许多基因组成的,可以大致分为三类:I类,II类和III类。参与抗原呈递和相关免疫应答的两种主要类型的HLA分子是I类和II类分子。HLA-I类包含HLA-A、-B、-C;HLA-II类包含HLA-DR、-DQ、-DP。对一个基因座位,一个个体最多只能有两个等位基因,分别来自父母方的同源染色体上,因而一个个体的免疫细胞的表面通常可以检测到分别来自父母双方6对共12种HLA Ⅰ类和Ⅱ类等位基因分子即HLA抗原。
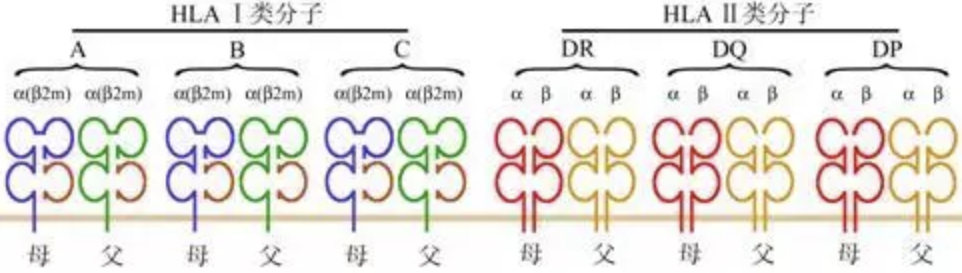
图:细胞表面呈共显性表达的6对12种经典Ⅰ类和Ⅱ类HLA分子
HLA基因遵循孟德尔遗传学的规律,编码的抗原在细胞表面具有共显性表达特点,即同源染色体对应座位上的两个等位基因皆能得到表达。由于MHC基因位于同一条染色体上,其多基因座位上的基因型组合相对稳定,很少发生同源染色体间交换,这就构成了以单倍型(HAPLOTYPE,即在同一条染色体上紧密连锁的一系列等位基因的特殊组合)为特征的遗传。(在没有重组发生的情况下,HLA基因通常从每个亲本那获得整体遗传。HLA单倍型是在单个亲本染色体上传递的连接的HLA基因的组合。)
- 胚系及体系HLA检测
HLA检测分为两个层面,一个是患者胚系HLA基因分型,目的是看患者HLA的多样性,另外一个层面是看肿瘤细胞的HLA基因是否因为免疫逃逸发生了杂合性缺失,前者检测的是患者的正常细胞如血液白细胞提取的DNA,后者检测的是肿瘤组织提取的DNA,HLA基因分型是HLA杂合性缺失分析的基础。
|
HLA检测 |
检测内容 |
检测样本 |
遗传性 |
|
胚系(Germline) |
HLA的遗传多样性(HLA分型) |
正常细胞(血液白细胞) |
可遗传 |
|
体系(Somatic) |
HLA杂合性缺失(somatic LOH) |
肿瘤细胞 |
不可遗传 |
肿瘤的发生与免疫系统的功能密切相关。研究表明,HLA LOH是在癌症进化晚期和在强大的选择压力下发生的。肿瘤中HLA LOH阳性会导致HLA基因功能丧失,更多地发生在癌症进化后期,晚期癌症更容易受到免疫逃逸机制选择。
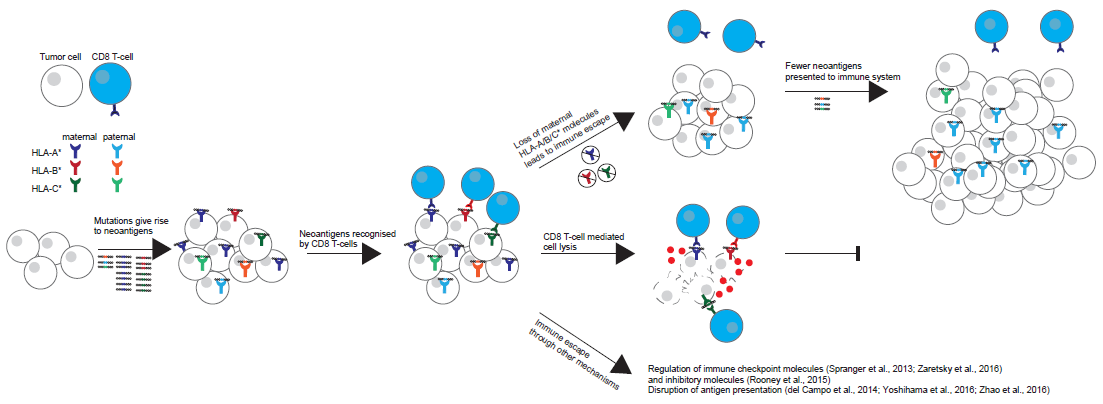
- 遗传性HLA等位基因分型——HLA的多样性
除同卵双生子以外几乎找不到HLA相同者,每个人的HLA千差万别,因此,HLA有人体生物学“身份证”之称。
- 一个完整的HLA等位基因由8个数字和1个字母组成,示意图如下:
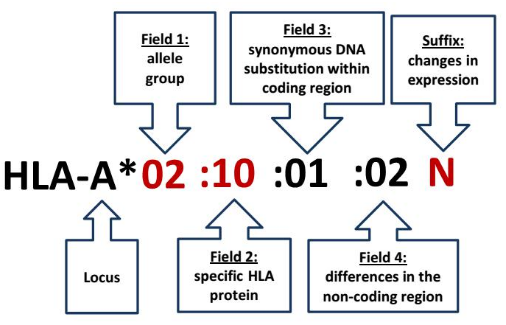
HLA是固定前缀,A代表基因座位;*星号作为分隔符,分隔符之后是同一个基因的不同allele,由冒号分隔的多个部分构成,最多包含4个部分,第一组”02”代表不同的等位基因组别,常指血清学特异性;第二组”10”代表一种特定类型的HLA蛋白;第三组的”01”代表发生在编码区的同义突变;第四组的”02”代表发生在非编码区的基因突变;最后的字母表示基因的蛋白表达状态。(不同后缀的含义不同,N表示该等位基因不表达,L表示该等位基因低表达,S表示该基因编码可溶性的分泌型蛋白;C表示该等位基因编码的产物存在于胞浆中;A表示异常表达的等位基因;Q表示有疑问而不能断定。)
HLA分型的分辨率可以分为以下四类:
a. 2位为等位基因;
b. 4位为特定HLA 蛋白质;
c. 6位为特定HLA基因编码区(CDS)的同义突变;
d. 8位为特定HLA基因非编码区的突变。
- HLA等位基因的分类
2007年美国组织相容和免疫遗传协会(ASHI)成立了一个特设委员会,提出常见及确认的等位基因表(Common alleles and well documented alleles,CWD)。
严格按照国际上最新版本文献对CWD等位基因的定义,将HLA等位基因定义为三大类:常见等位基因(Common alleles)、确认等位基因(Well-documented alleles)、罕见等位基因(Rare alleles)。
- 常见等位基因(Common alleles):在参考群体中频率等于或大于0.001的等位基因。
- 确认等位基因(Well-Documented alleles):指PCR-SBT方法检测中,那些至少在五个独立非亲缘个体中或者三个独立非亲缘个体中并伴有特定的单体型被检测到的等位基因。
- 罕见等位基因(Rare alleles):除常见等位基因和确认等位基因以外的所有等位基因。
CWD原则分型中将常见等位基因和确认等位基因合并为CWD,当模棱两可的等位基因组合中出现CWD等位基因需要进一步区分,而出现罕见等位基因组合其临床分型中实际意义有限可予以排除。
HLA基因分布具有人群特性,不同人群、地区HLA等位基因出现的频次存在差异,中华骨髓库(China Marrow Donor Program,CMDP)组织国内HLA领域有关专家制订了中国人群的(CWD表>,对我国HLA实验室常规基因分型工作具有重要的指导意义。
最新版参考:中国常见及确认的HLA等位基因表(CWD)2.2版本
- HLA分型检测方法
HLA分型被定义为I类和II类基因座的多态性。血清学是一种传统的HLA的分型方法。分子检测方法的兴起减弱了利用携带所有HLA抗原相应抗体的血清来进行HLA分型的必要性。HLA基因分型技术是近年来发展起来的一种分子生物学技术。
基于测序的分型(Sequence-based typing,SBT):该技术可在多个不同平台上进行,一种是基于Sanger的DNA测序,另一种是基于NGS的测序。该方法的最常见应用是鉴定干细胞移植受体和供体的等位基因水平上的HLA分型。等位基因一般指位于一对同源染色体的相同位置上控制着相对性状的一对基因,是基因上独特的核苷酸序列。该方法允许确认新的等位基因序列。
目前世界卫生组织推荐的HLA分型方法的“金标准”是PCR-SBT(polymerase chain reaction-sequence specific primer),检测座位覆盖HLA-A、-B、-C、-DRB1和-DQB1,广泛应用于临床移植供受者HLA基因分型。然而由于HLA基因高度多态性和检测技术的限制,在检测特定座位的分型中存在模棱两可的等位基因分型结果。模棱两可的基因型结果是指在HLA基因分型过程中,标本指定结果中存在一种以上的HLA等位基因组合方式。
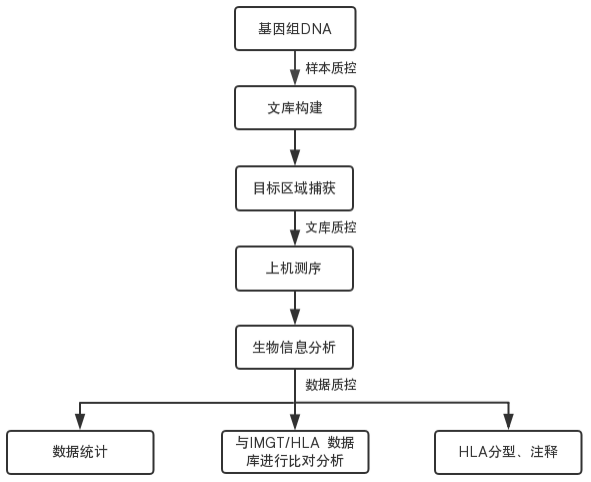
由于NGS测定序列为单链结果,因此有助于解决经典双链测序存在的模糊指定问题。所以虽然我们对新生抗原认识时间已经不短了,但近几年随着NGS技术的发展以及配套生物信息分析的完善,才有可能对大量突变的新生抗原进行识别和鉴定。通过二代测序数据分析进行HLA分型,可获得小至单个SNV 基因型的多态性,大至单体型信息。通过捕获测序技术,可针对MHC区域进行捕获,使得测序深度和准确性更高。NGS技术在HLA分型中的实验基本流程包括:模板制备、PCR体系扩增、产物均一化、测序反应、数据分析。NGS技术在HLA分型中具有高通量和高准确性,而且试剂成本明显降低,但应注意到在NGS检测过程中可存在HLA等位基因扩增不平衡和丢失现象。
二代测序对HLA分型的流程图:
- HLA基因的杂合性缺失——肿瘤免疫逃逸
LOH(Loss Of Heterozygosity,杂合性缺失):正常情况下,常染色体上的一个区段,都会有来自于父亲、和母亲的各一个拷贝。当发生杂合性缺失(LOH)的时候,两个染色体上的同一个区段,都是来自于或者父亲、或者母亲的一方,而把另一方的对应区段给丢失了。这就叫杂合性缺失(LOH)。
“单亲二体型”,也就是“Uniparental Disomy”,简称“UPD”,是杂合性缺失的一种特殊形式。也就是一对染色体,都是来自于父亲、或者母亲中的一方,而把另一方的对应染色体,全部给缺失了。这种变异的危害,和杂合性缺失的道理是一样的。只是因为它丢的是一整个染色体,所以致病的可能性会更高。
HLA基因LOH阳性代表着HLA基因存在杂合性缺失,HLA功能受损。由于HLA的功能是呈递新生抗原到细胞表面,供T细胞识别的,故一旦功能部分或者完全缺失,会导致抗原呈递能力缺失,免疫系统无法识别肿瘤的情况,即肿瘤易于免疫逃逸,也就是说这个患者可能存在对免疫药物耐药的风险。HLA LOH是肿瘤细胞在面对免疫系统的攻击下产生的一种自我保护的免疫逃逸机制,使其无法被T细胞识别及杀伤,从而可能造成肿瘤细胞中的突变累积。HLA杂合性缺失导致的免疫逃逸是免疫治疗需要克服的一个重要障碍。
- 新生抗原
- Neo-Antigen(新生抗原):能激活免疫系统的、由癌细胞基因突变所产生的、携带有特异性氨基酸序列变异异常蛋白质,能够被HLA分子呈递突变并诱发T细胞应答。这是因为如果没有氨基酸序列的改变,这些蛋白应该是没有抗原性的。
新生抗原是一种位于肿瘤细胞表面的特异性抗原,具有肿瘤特异性,是癌基因体细胞突变(Somatic mutations)编码的含有突变氨基酸的抗原肽,不存在于正常细胞中,因此免疫系统可以将其识别为“非自体”抗原并引起免疫应答,并且不受免疫耐受的影响。这使其成为免疫治疗的理想靶点。新生抗原仅来源于肿瘤特有的体细胞突变形成的蛋白,具有个体差异性和肿瘤特异性,能够被T 细胞识别并引起特异性的免疫应答,在个性化免疫治疗领域拥有广阔前景。
肿瘤新抗原作为免疫治疗的靶点主要优势包括无中枢耐受、与主要组织相容性复合物(MHC)分子亲和力强、降低了正常组织的脱靶副反应、安全性高等。
当新生抗原在细胞内部时,它们被切割成肽,并且这些肽与I类或II类分子结合,然后HLA分子可以在细胞表面呈递可被T细胞受体识别的肽段。HLA I类和II类分子将源自病原体的短肽(如肿瘤新生抗原)呈递给T细胞以启动适应性免疫应答。新生抗原在免疫治疗中起效的根本原因是,新生抗原能够激活免疫细胞来识别杀伤肿瘤细胞。
- 肿瘤新生抗原预测
越来越多的证据表明,肿瘤WES鉴定的非同义突变中只有一小部分能够产生具有免疫原性的新生抗原。新生抗原鉴定的成败在很大程度上取决于候选新生抗原的鉴定和新生抗原免疫原性的评估。
肿瘤新生抗原预测涉及两个主要关键点,一是对患者的HLA分子进行分型;二是鉴定和选择合适的体细胞突变。肿瘤新生抗原预测一般需要精确到四位数的HLA 亚型。
如何更好地从基因组数据中鉴定免疫原性新抗原是目前待解决的重要问题之一。事实上,至少有两个影响肽免疫原性的生物物理结合事件:肽-MHC结合和TCR识别肽-MHC复合物。目前的方法可分为两种:一种是预测突变肽段跟HLA分型的结合亲和力,另一种是预测T细胞的TCR识别新生抗原的潜力。
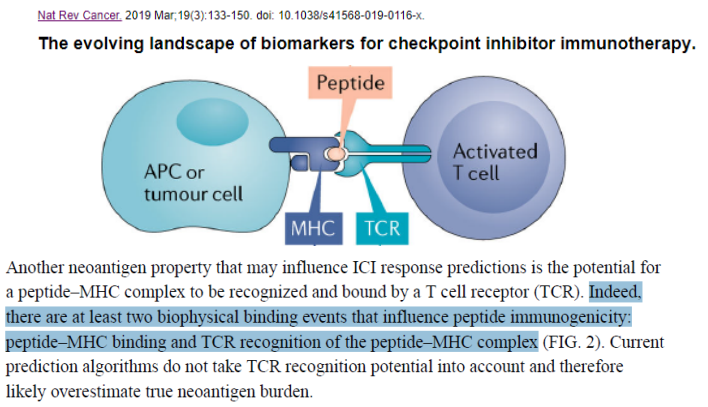
选择新生抗原时优先考虑:测序深度深、突变频率高、mRNA表达信号强、新生抗原的亲和力(半数最大抑制浓度IC50)小(说明与HLA分子结合越强)、新生抗原与其对应野生型多肽的亲和力之比小(意味着新生抗原与HLA分子结合能力远远强于相应野生型多肽与HLA分子的结合力)的新生抗原,此外还需要综合考虑产生新生抗原的突变基因的生物学功能,尤其是与所研究疾病的关联性。
- 肿瘤免疫治疗三驾马车:免疫检查点抑制剂、过继细胞治疗、个性化肿瘤疫苗
癌症免疫疗法是一种利用免疫细胞,增强免疫细胞的功能来消除癌症的治疗方式。它可以:帮助免疫系统识别和攻击特定的癌细胞;增强免疫细胞,消灭癌症;为身体提供额外的物质增强人体免疫反应。
我们通常所说的免疫治疗技术主要有以下三种:
免疫检查点抑制剂:通过抑制肿瘤细胞的免疫逃逸,调动自身免疫系统来消除肿瘤,代表为CTLA-4/PD-1/PD-L1单抗。
肿瘤ACT疗法(adoptive cell therapy,过继细胞治疗)是指向患者输入在体外培养激活的、具有抗肿瘤活性的的免疫细胞,借助它们直接杀死或者激活机体免疫系统消灭肿瘤细胞,最终实现治疗肿瘤的目的,代表为CAR-T/TCR-T。携带肿瘤特异性抗原(肿瘤新生抗原/Neoantigen)的过继性细胞,能够特异性的激活携带Neoantigen的T细胞,以针对性的杀死肿瘤细胞。
个性化肿瘤疫苗是指将肿瘤新生抗原(neoantigen)的肽段或RNA注入患者体内,在体内激活患者的免疫系统,实现杀伤肿瘤的效果。个性化肿瘤疫苗技术的突破,关键在于neoantigen的检测及预测技术的发展,以制备neoantigen疫苗。
到目前为止,针对新生抗原的临床试验疫苗已被证明安全且耐受良好,针对新生抗原的个性化T细胞疗法也显示出抗肿瘤反应。
总结:基于新生抗原的肿瘤免疫治疗具有以下几点优势:(1)新生抗原只在肿瘤细胞表达,无遗传性;(2)该疗法只激活个体自身的免疫系统,并未导入病毒等个体中原先不存在的物质,风险小;(3)靶向准确性高。
注:TCR(T cell receptor,T细胞受体)和CAR(chimeric antigen receptor,嵌合抗原受体)T细胞疗法都对患者自身的T淋巴细胞在体外进行改造,然后将它们注回患者体内杀伤肿瘤的癌症疗法,但是它们识别抗原的机制截然不同。TCRs利用α和β肽链构成的异元二聚体(heterodimer)来识别由MHC(主要组织相容性复合体)呈现在细胞表面的多肽片段。而CARs则利用能够与特定抗原结合的抗体片段来识别肿瘤细胞表面的抗原,包括肿瘤特异性抗原(tumor-specific antigen, TSA)和肿瘤相关性抗原(tumor-associated antigen, TAA)。CAR-T细胞治疗血液肿瘤方面获得了极大的发展,但CART疗法的效果在实体瘤上则显得没有那么乐观,主要问题是因为它们的靶点抗原都是细胞表面蛋白,而实体肿瘤的抗原表达具有高异质性,如何在实体瘤中选择合适的CAR-T细胞靶点是研究者面临的挑战。在治疗实体瘤方面,TCR疗法可能比CAR疗法更有优势。
- 免疫治疗预后biomarkers之人类白细胞抗原(HLA)、新抗原
|
人类HLA类基因多样性 |
HLA类基因多样性越多,T细胞识别肿瘤能力就越强;而多样性明显丧失,识别能力就会下降,免疫治疗的疗效也会降低。 |
|
HLA杂合性缺失(LOH) |
HLA基因的等位基因的杂合性越高,患者治疗预后更好。HLA纯合等位基因的患者或者杂合性缺失(LOH)的患者接受免疫检查点抑制剂治疗的效果较差。HLA LOH是癌症进化中应对强选择的一种免疫逃逸机制。 |
|
TMB结合HLA LOH |
TMB结合HLALOH共同分析,更精准地筛选高获益人群。晚期肿瘤可能选择HLA LOH作为其免疫逃逸的机制,因此如果只是单纯检测TMB,根据TMB高的结果给出用药建议,可能会使得这部分的患者出现免疫治疗无效的情况。 |
|
肿瘤新抗原负荷(TNB) |
肿瘤突变负荷(TMB)升高会增加产生新抗原的机会从而引起免疫原性。真正的肿瘤新抗原负荷(TNB)与TMB相比可能与ICI治疗反应具有更强的关系。 |
|
Neo-Antigen(新生抗原) |
一般而言,患者肿瘤组织中基因突变的总数越多(也就是TMB越高),那么所携带的neoantigen也越多,能够被T细胞的TCR特异性识别的概率越大,新抗原疫苗对肿瘤部位免疫杀伤活性越大 |
注:TNB(Tumor Neoantigen Burden),即肿瘤新生抗原负荷,是反应肿瘤细胞中总的新生抗原数量的一个指标,通常以每百万碱基中(Mb)的肿瘤基因组区域中包含的肿瘤新生抗原的数量来表示。TNB可能在癌症免疫治疗中形成一种生物标志物,并为开发新的治疗方法提供动力,从而选择性地增强T细胞对这类抗原的反应活性。
参考文献:
[1] 中华骨髓库CWD表2.2版本.
[2] 陈碧清,孔祥图,徐祖琼,代兴斌,于菊华,朱学军.原发性浆细胞白血病肿瘤新生抗原的筛查和预测[J].中国肿瘤生物治疗杂志,2019,26(07):730-735.
[3] Havel, J. J., D. Chowell and T. A. Chan (2019). "The evolving landscape of biomarkers for checkpoint inhibitor immunotherapy." 19(3): 133-150.
[4] McGranahan, N., et al. (2017)."Allele-Specific HLA Loss and Immune Escape in Lung Cancer Evolution." Cell 171(6):1259-1271 e1211.
[5] Chowell, D. and L. G. T. Morris (2018). "Patient HLA class I genotype influences cancer response to checkpoint blockade immunotherapy." 359(6375): 582-587.
HLA系统具有高度遗传多态性,是机体内特异性免疫识别和免疫应答的主要组成成分。多态性 (polymorphism) 指一个基因座位上存在多个等位基因 (allele),是一个群体概念,指群体中不同个体在等位基因拥有状态上存在差别。(多基因性着重于同一个个体中HLA基因座位的变化;而多态性指群体中各座位等位基因数量的变化)




