2025-07-25 09:51:54
2025年7月10日NCCN发布了最新的一期非小细胞肺癌指南V7.2025,在本次更新中,将舒沃替尼(Sunvozertinib)加入,作为EGFR基因20号外显子插入突变(后文用EGFR Exon20ins简写)阳性的晚期或转移性非小细胞肺癌(NSCLC)患者的后线治疗选择,适用于一线治疗方案进展后的患者群体[1]。而该方案则在更早些时候于2025年7月2日由FDA加速获批,成为目前全球首个且唯一在美获批的EGFR Exon20ins的非小细胞肺癌国产创新药[2]。

NCCN非小细胞肺癌指南V7.2025

2025年7月2日FDA批文
舒沃替尼的加速获批及指南写入,是基于WU-KONG1B(NCT03974022)的II期临床试验研究。该研究是一项国际多中心、开放标签、剂量随机化的临床试验,入组患者为经含铂化疗后疾病进展的局部晚期或转移性EGFR Exon20ins突变非小细胞肺癌(NSCLC)患者,评估数值包括客观缓解率(ORR),次要终点包括评估的缓解持续时间(DOR)。
试验入组患者被1:1随意分配为两个组别,分别每日服用200 mg和300 mg舒沃替尼疗,疗效可评估人群为85例服用200 mg/天的患者。入组人员中有46%的患者得到缓解,其中完全缓解6%,部分缓解40%,疗效中位持续时间为11.1个月。
相较于今年7月份的FDA批准以及写入NCCN指南,舒沃替尼作为一款自主研发的国产肺癌靶向药,早在2023年8月就经NMPA批准上市,并在2024年4月写入国内的CSCO指南。同时,于2025年1月1日起,舒沃替尼也被纳入了医保名录中。
然而,与EGFR基因更为常见的L858R突变或是19号外显子缺失突变的药物相比,针对于Exon20ins的靶向药要少得多。这两年隔壁时不时的就崩出来一款新的L858R/19del的药物,或是适应症直接针对于T790M的三代药,本就已经十分拥挤的靶向药赛道更是挤满了参赛选手。反观Exon20ins适应症的药物,从2021年9月FDA首次批准莫博赛替尼(Mobocertinib),到24年3月FDA再次批准埃万妥单抗联合卡铂和培美曲塞用于EGFR Exon20ins的局部晚期或转移性非小细胞肺癌一线治疗,哪怕再加上舒沃替尼,全球携带EGFR Exon20ins突变的NSCLC患者可选的药物也着实有限。雪上加霜的是,23年10月莫博赛替尼在III期临床实验中未能显著延长无进展生存期(PFS),武田制药主动提出退市[3][4]。所以市面上目前患者可选的获批药物仅只有埃万妥单抗和舒沃替尼两款。

FDA接受武田制药主动提出的莫博赛替尼退市申请
同年莫博赛替尼于中国市场退市
除了上述两款获批药物,目前在开展的Exon20ins临床试验并不算多,毕竟相对于人群更庞大的L858R/19del携带患者,20号外显子插入突变的检出率即使在EGFR高发的中国人群中也只占了非小细胞肺癌的0.3-2.9%[5],可获及的比率并不算高。但毕竟中国人口基数大,随着老龄化的加剧以及基因检测的普及,对于该突变大类及其亚型还是有相当大的需求人数。
目前在处于临床试验阶段的药物CLN-081(Zipalertinib)在今年5月份ASCO会议上披露了其REZILIENT1研究的2B期数据。该研究中将患者分为既往含铂化疗和既往含铂化疗联合埃万妥单抗两个队列,并接受100mg每日两次的Zipalertinib治疗。入组的176名患者中有51例过往接受过埃万妥单抗的治疗,在中位随访9.3个月的评估结果中,总体人群确认客观缓解率(cORR)为35.2%,中位缓解时间(mDoR)达8.8个月,中位无进展生存期(mPFS)为9.5个月。过往未接受过埃万妥单抗治疗的125名患者的cORR为40.%,中位DoR同为8.8个月;另外51名接受过埃万妥单抗的人群中,细分为30例未接受其他Exon20ins靶向治疗(cORR为30.0%)和21例曾接受过其他Exon20ins组(如莫博赛替尼、舒沃替尼、BLU-451等,cORR为14.3%)。Zipalertinib已获得FDA的突破性疗法认证,在未来上市后或许能给既往接受或埃万妥单抗亦或是舒沃替尼的患者带来更多的希望。[6]
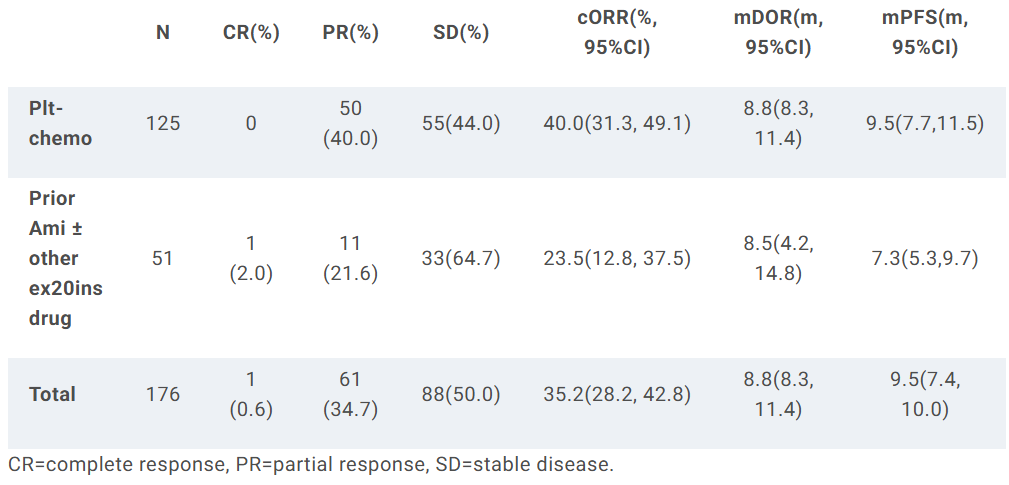
CLN-081(Zipalertinib)于2025年ASCO会议披露REZILIENT1研究数据
其他目前处于临床阶段的药物还包括ABSK112、Poziotinib、YK-029A等,期待有更多殷实可靠的临床数据披露。
与常见EGFR基因L858R和19del突变大类相比,20ins的亚型更为复杂,普通的PCR方法无法包含所有的突变类型,因而临床上更适合用NGS方法进行检测。针对EGFR基因各类型变异及其他肺癌热点基因,魏尔啸医学检验实验室可提供多个检测项目供临床选择,用于辅助临床靶向、免疫、化疗药物的可能获益预测。
以下为部分适用检测项目:
- 肺癌靶向17基因检测,样本类型:组织/外周血/胸腹水/脑脊液
- 肺癌精准治疗107基因检测,样本类型:组织/外周血/胸腹水/脑脊液
- 实体瘤靶向66基因检测,样本类型:组织/外周血/胸腹水/脑脊液
- 实体瘤精准治疗180基因检测,样本类型:组织/外周血/胸腹水/脑脊液
- 实体瘤精准治疗715基因检测,样本类型:组织/外周血/胸腹水/脑脊液
参考来源:
[1] NCCN非小细胞肺癌指南V7.2025
https://www.nccn.org/professionals/physician_gls/pdf/nscl.pdf
[2]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-sunvozertinib-metastatic-non-small-cell-lung-cancer-egfr-exon-20
[3]https://www.federalregister.gov/documents/2024/07/15/2024-15371/takeda-pharmaceuticals-usa-inc-withdrawal-of-approval-of-new-drug-application-for-exkivity
[4]https://www.takeda.com.cn/statements/2024/announcement-for-exkivity-in-china/
[5]Burnett H, et al. Epidemiological and clinical burden of EGFR Exon 20 insertion in advanced non-small cell lung cancer: A systematic literature review. PLoS One. 2021 Mar 8;16(3):e0247620. doi: 10.1371/journal.pone.0247620
[6]https://meetings.asco.org/abstracts-presentations/247323




